Crónica de la VI mHealth BCN Conference: Salud digital, del hype al mundo real

El pasado jueves 15 de febrero tuvo lugar la VI mHealth BCN Conference sobre “Salud digital, del Hype a la realidad” en el espacio Can JaumeAndreu de la UOC, organizada con la colaboración del eHealth Center (UOC), la Sociedad Catalana de Medicina Familiar y Comunitaria (CAMFiC) y el Hospital Clínic de Barcelona. La edición de este año "La salud digital del Hype a la realidad", la dedicamos a explorar la diferencia entre los deslumbrantes hypes de la tecnología digital y sus dificultades de aplicación en el mundo real.
La jornada se inició con la inauguración por parte de Imma Grau, presidenta de la Fundación iSYS, internet, Salud y Sociedad, Marta Aymerich, presidenta del Consejo de Dirección del eHealth Center (UOC), Antoni Sisó i Almirall, presidente de la Societat Catalalana de Medicina Familiar i Comunitaria (CAMFiC) y Araceli Camacho, responsanle del Plan de Transformación Digital del Hospital Clínic de Barcelona.

La conferencia inagural la impartieron los fundadores de Social Diabetes. En la primera mesa se debatió entre los beneficios de las apps en la adopción de comportamientos saludables y la necesidad de desconexión digital para mejorar la salud y prevenir las adicciones. En la segunda se destacaron las dificultades de introducir la salud digital en el sistema de salud, las novedades en la evaluación de las tecnologías digitales, en la acreditación y la importancia de incorporar el punto de vista del paciente. Por último, se dieron a conocer los ganadores de la X edición del TOP5 de Apps de salud según el iSYScore.
Social Diabetes
Víctor Bautista (CTO) y Maria Jesús Salido (CEO), ambos fundadores de Social diabetes, estuvieron a cargo de la conferencia inagural. Víctor, en el año 2008, mientras vivía en Londres, fue diagnosticado con diabetes tipo 1, y decidió regresar a Barcelona para estar más cerca de su familia. Impactado por las limitaciones y la falta de tecnología en el manejo de su condición y motivadao a mejorar su calidad de vida, comenzó a desarrollar una aplicación personalizada para gestionar su diabetes. Los resultados positivos y el encuentro con María Jesús, le inspiraron a compartir su programa con otros pacientes y médicos, y crearon SocialDiabetes. Eran tiempos con pocas regulaciones y sin un mercado maduro (tenían "un ferrari para caminos de tierra") cuando inició su singladura esta startup barcelonesa.
Durante la conferencia se centraron en cuatro elementos fundamententales esn el desarrollo y la supervivencia de su empresa: Producto, mercado, regulación y equipo.

Salud digital y desconexión digital: utilidad vs wellbeing
A continuación, se presentó la mesa redonda moderada por Manuel Armayones (director del Behavioral Design Lab del eHealth Center de la UOC). La mesa contó con la participación de la Dra. Dominica Díez Marcet (PhD, Psicòloga Clínica, Unitat d'Addiccions Comportamentals, Fundació Althaia i professora de la UVic-UCC) que habló sobre la evolución del uso de pantallas en jóvenes y adolescentes, la Dra Eva Rimbau (PhD, Professora de Direcció de Persones a la UOC), cuya participación se centró en como facilitar la desconexión digital en el trabajo, y la Dra. Carme Carrion (PhD. Investigadora Principal grup de recerca eHealth dels Estudis de Salut UOC), que contestó a la pregunta sobre si las Apps pueden ayudar en el manejo de la depresión.

Introducción de la salud digital en el sistema sanitario, acreditación, evaluación y disponibilidad.
La segunda mesa redonda, fue moderada y presentada por Jordi Acezat (Médico de Familia, adjunto Dirección SAP Montaña-Derecha BCN-APiC, Dir ESIC Casernes, vocal innovación Junta permanente CAMFIC) que co-creó un grupo de Salud Digital en CAMFiC para generar evidencia, mejorar las competencias digitales de los profesionales de salud y contribuir a empoderar a los pacientes usuarios de estas tecnologías. Propuso la necesidad de garantizar calidad, seguridad y eficiencia e integrar las tecnologías digitales dentro de un marco normativo/regulador para poder emplearlas. Dado que a partir de los resultados que ofrezcan los desarrollos de mHealth, va haber un acto médico, señaló la necesidad de que estas características concurran. También apuntó la necesidad de la interoperabilidad y compartición de datos, el mantenimiento y adaptación continuada, además de la equidad en el acceso.
La Dra.Sandra Garcia Armesto (Investigadora de Sistemas y Políticas de Salud. Directora de l'Agència de Qualitat i Avaluació Sanitàries de Catalunya -AQuAS) presentó el progreso hacia un modelo europeo de evaluación de tecnologías sanitarias (HTA-Regulation), detallando el marco de evaluación de tecnologías sanitarias: adaptación para la evaluación de tecnologías de salud digital, recientemente desarrollado bajo el liderazgo de AQuAS; la Dra. Caridad Pontes (Farmacóloga clínica) nos explicó el proceso de digitalización de la prestación farmacéutica del cual ella ha sido impulsora; el Sr. Jordi Escudero (Director de Digital Health en Evidenze) habló sobre las diferencias entre salud digital y digital therapeutics y de su abordaje. Por último la Sra. Elisenda de la Torre (Patient advocate) que explicó el rol de los patient advocate y su rol en salud digital. El debate posterior fue muy enriquecidor.

Aplicaciones de Salud Digital: ¿recesión del mercado?
Por último, Imma Grau, y Ángeles Fuentes, de la Fundación iSYS, presentaron la décima colección de Apps de Salud y el TOP5 de Apps 2023-2024 para pacientes y para profesionales según los criterios de iSYS. Preventicus Heartbeats y Diabetes M, las mejores Apps para pacientes en la décima edición del ranking iSYScore.
Vídeo de la jornada
¡Gracias a tod@s!
Fotografías: Juan José Lacalle
Video: Jordi Alcalá
 Redacción -Fundación iSYS
Redacción -Fundación iSYS
Preventicus Heartbeats y Diabetes M, las mejores Apps para pacientes según el ranking iSYScore 2024
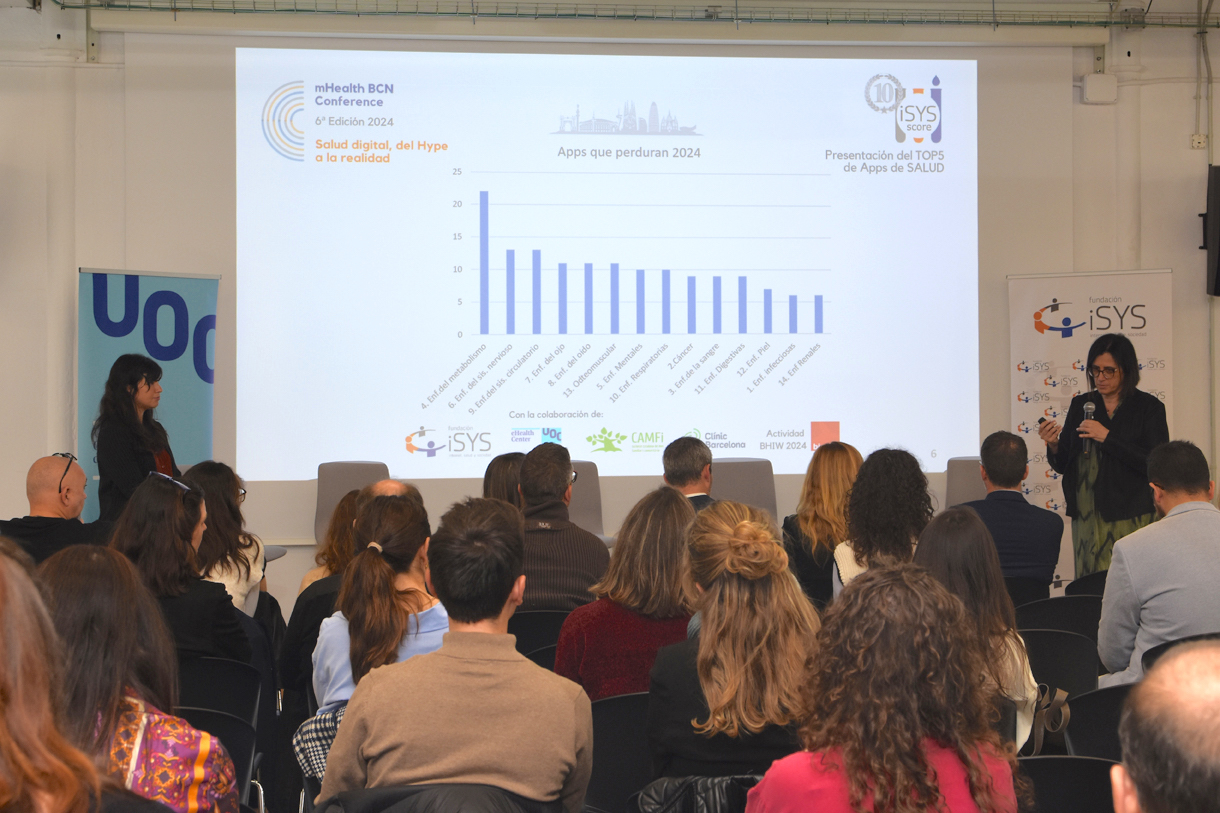
El pasado 15 de febrero de 2024, la Dra. Imma Grau, presidenta de la Fundación iSYS, junto con la responsable de I+D+i, Ángeles Fuentes dieron a conocer las Top 5 Apps de Salud 2023/2024 valoradas según el iSYSCore. La presentación se produjo durante la VI Edición de la mHealth Barcelona Conference sobre “Salud digital, del Hype a la realidad”, organizada en colaboración con el eHealth Center de la UOC, la CAMFiC y el Hospital Clínic de Barcelona.
Las Apps clasificadas en primer lugar han sido: Preventicus Heartbeats (certificada como dispositivo médico para registrar la frecuencia cardíaca mediante la cámara de un teléfono inteligente o fotopletismografía) y Diabetes M (gestión de la diabetes), en la categoría general para para pacientes. En la categoría Best in Class, que reconoce a las apps que han encabezado el ranking durante más de tres años, encontramos a Social Diabetes y One Drop.
El ranking de mejores Apps se elabora con las escalas iSYScore, un método único y objetivo, desarrollado por expertos y publicado en las revistas científicas, que permite evaluar y puntuar aplicaciones para pacientes y profesionales de la salud, valorando la confianza, utilidad e interés popular. Se evalúan Apps en español y catalán, que cumplen una serie de criterios de inclusión y una puntuación mínima según la escala de iSYScore.
“Este año hemos observado un retroceso en la aparición de nuevos desarrollos y la desaparición de algunos clásicos”, precisa Imma Grau, fundadora y presidenta de la Fundación iSYS. Y afirma que “las nuevas reglamentaciones garantistas de la UE, que este año llegarán a seis, pueden dificultar desarrollos de emprendedores con recursos escasos. También las nuevas políticas de las plataformas, más restrictivas, pueden incidir en este retroceso. Estaremos atentos a la adaptación a este nuevo contexto.”
Para esta edición del TOP5, la Fundación iSYS ha examinado 301,de las que 51 pasaron los criterios de inclusión y 33 superaron la nota de corte y constituyen las recomendaciones de este año, 23 Apps en el apartado general y 10 Apps en el “Best in Class”.
Durante los diez años de realización del ranking iSYScore, los expertos de la Fundación iSYS han valorado más de 3.200 Apps, seleccionado un total de 233, de las que 147 siguen estando disponibles.

Listado de recomendaciones 2023-24 (una misma clasificación significa que han obtenido la misma puntuación):
Top 5 pacientes
1 Preventicus Heartbeats
1 Diabetes:M - Blood Sugar Diary
2 OWise - Cáncer de Mama
2 SkinVision
3 Ada – tu guía de salud
4 Migraine Buddy - dolor de cabeza y migraña
4 FreeStyle LibreLink
4 Yana: tu acompañante emocional
4 Hailie Manejo del asma y la EPOC
5 PreParaDXS
5 MicroHealth Hemofilia
5 Cardio Signal
Top 5 “Best in Class”
1 SocialDiabetes
1 One Drop: Gestión de Diabetes
2 mySugr: App Diario de diabetes
2 Contour diabetes
3 Propeller
3 Fibricheck
4 Cancer.net
5 Nefrodiet
https://www.fundacionisys.org/es/apps-de-salud/catalogo-de-apps
 Redacción -Fundación iSYS
Redacción -Fundación iSYS
X Edición del TOP5 y el catálogo anual de Apps de Salud de la Fundación iSYS

El plazo de inscripción finalizará el 15 de diciembre.
La Fundación iSYS tiene entre sus objetivos contribuir a la mejora de la salud y la calidad de vida de los ciudadanos a través de la búsqueda de las mejores prácticas en salud digital. En esta línea nació, en 2014, el catálogo anual iSYS de Apps de salud, para facilitar el acceso a apps de interés, confianza y utilidad, valoradas con baremos objetivos y consensuados con expertos (el iSYScore PAC para las Apps destinadas a pacientes y iSYScore PRO para las de profesionales). Las Apps que estén en nuestro catálogo serán publicitadas por diferentes medios y formarán parte de nuestro informe anual de recomendaciones. Desde 2019 incluimos un apartado dedicado a las Apps "Best in Class", que incluye a las apps que han estado más de tres años en el Top5 y que continúan cumpliendo los criterios de calidad.
Crónica de la V mHealth BCN Conference: Ética y salud digital

El pasado jueves 23 de marzo tuvo lugar la V mHealth BCN Conference sobre “Ética y salud digital” en el Movistar Centre organizada con la colaboración del eHealth Center (UOC), y la Sociedad Catalana de Medicina Familiar y Comunitaria (CAMFiC).
Sobre la ética en el desarrollo de las tecnologías de salud digital, se abordó por un lado el uso de los datos personales de salud en la construcción de valor y, por otro, el uso de técnicas persuasivas para conseguir el objetivo de inducir conductas saludables.

La jornada se inició con la inauguración por parte de Imma Grau, presidenta de la Fundación iSYS, internet, salud y sociedad, con Marta Aymerich, presidenta del Consejo de Dirección del eHealth Center (UOC) y Antoni Sisó i Almirall, presidente de la Societat Catalalana de Medicina Familiar i Comunitaria (CAMFiC)
El reciente ciberataque ransomware sufrido por el Hospital Clínic de Barcelona, mencionado por Sisó, señala la importancia de optimizar la protección, la seguridad y la confidencialidad de los datos de salud.
La vida inmortal de Henrietta Lacks (HeLa)
Jordi Rambla, profesional del Center of Genomic Regulation, inició su conferencia con la historia de Henrietta Lacks. La Sra Lacks enfermó de cáncer mediados del siglo pasado, ella no sobrevivió, pero sus células cancerosas si lo hicieron y facilitaron nuevas líneas de investigación médicas y grandes hallazgos. Pero Lacks nunca autorizó el uso de sus células, y años después, cuando se desentrañó el genoma, su información y la de sus familiares quedó disponible de forma libre.
Rambla apuntó, que en la actualidad y a pesar de la reglamentación, es difícil asegurar totalmente la confidencialidad. Presentó algunos de los protocolos que se están estableciendo a nivel europeo para poder compartir datos y aprender de ellos mediante el análisis y la comparación. El proyecto Beacon, es un ejemplo en red que permite un acceso selectivo a la información, con intercambio de datos mediante la compartición progresiva y con un acceso restringido a personal o instituciones autorizadas.

La ética debe acompañar a la ciencia observando los riesgos
A continuación, se presentó la mesa redonda sobre Ética en el uso de datos, moderada por Rosa Morros, presidenta del Comité Ético de Investigación Clínica IDIAP Jordi Gol. La mesa contó con la participación de Montserrat Esquerda, Directora General del Institut Borja Bioètica, Universitat Ramon Llull, que comentó las dificultades del uso secundario de los datos clínicos; de Diego Hidalgo-Mazzei, Psiquiatra, investigador del Hospital Clínic-IDIBAPS que presentó el proyecto PRESTO-CLINIC (que hace un uso exhaustivo de datos de pacientes), y las vicisitudes de llevar adelante un proyecto de estas características; y de Manuel Medina, Médico de Familia ICS, responsable del Sistema de información de los servicios de atención primaria (SISAP), que explicó como para convertir los datos en información, en SISAP emplean dos herramientas de gestión clínica: una Micro (para profesionales) i Macro (para EAP y entitades).
Esquerda señaló la puerta que se atraviesa cuando se emplean datos asistenciales para la investigación (uso secundario de datos clínicos). Explicó diversos métodos de autorización, recordando que los datos pertenecen a las personas. La importancia de la gobernanza de los datos para intentar garantizar la voluntad de sus propietarios, al tiempo de permitir un uso beneficioso de los mismos. Privacidad personal y uso en investigaciones científicas para el bien social. La ética no debe poner límites a la ciencia, pero debe salvaguardar a las personas de los riesgos, garantizando la confidencialidad y la privacidad. El usuario debe estar informado y poder de decidir cuando y en qué situaciones debe autorizar un nuevo uso de sus datos.

Persuasión o manipulación
La segunda mesa redonda, moderada por Elena Torrente (subdirectora de desarrollo de Salud Digital en DKV, donde es responsable del Innolab), reunió a expertos en tecnología y diseño del comportamiento para debatir, entre otros aspectos, sobre la frontera entre la persuasión y la manipulación explicada por Manuel Armayones, (director del Behavioral Design Lab del eHealth Center de la UOC), el soporte a toma de decisiones y importancia del diseño la información por Yasmina Okan (investigadora Ramón y Cajal en el Departamento de Comunicación de la Universidad Pompeu Fabra ) y la influencia del diseño en experiencia de usuario por Adrián Dorado (Co-fundador Qualud), teniendo en cuenta dimensiones biológicas, emocionales y conductuales.
Armayones definió el concepto de diseño persuasivo como el diseño de la influencia en el comportamiento para conseguir que alguien haga algo que quiere hacer y que le hace sentir bien, es decir, se trata de una persuasión positiva (dejar de fumar, caminar más, etc.). Se utiliza lo mismo para manipular que para persuadir: generar hábitos. El objetivo es ser capaces de utilizar esos métodos para la promoción de la salud.

Okan recomendó herramientas como la International Patient Decision Aids Standards (IPDAS), que establece los criterios básicos para desarrollar una herramienta de ayuda a la toma de decisiones.
Aplicaciones de Salud Digital: los chatbots entran en escena
Por último, Imma Grau, y Ángeles Fuentes, de la Fundación iSYS, presentaron la nueva colección de Apps de Salud y el TOP5 de Apps 2022-2023 para pacientes y para profesionales según los criterios de iSYS.
Vídeo de la jornada
¡Gracias a tod@s!

Fotografías: Juan José Lacalle
Video: Jordi Alcalá


